骨组织的退行性变、创伤、肿瘤、磨损是目前常见的骨科疾病,并严重影响患者生活质量,利用骨植入物对受损骨组织进行重建是治疗骨科疾病最常规有效的手段[1]。随着我国老龄化进程的加速以及肥胖率的增加,再加上政策扶持以及社会观念转变,中国骨科植入物市场尤其是硬组织植入物市场飞速发展。近年来,随着“精确诊疗”概念的普及,临床对骨科植入物提出了个性化的需求,骨科植入物要根据患者及使用场景实现外形尺寸以及内部结构的“量体裁衣”[2-3]。除了满足个性化的需求外,为了使植入物具有良好的初期稳定性和远期稳定性,常常需要在植入物表面构建骨小梁多孔结构,便于细胞的生长以及营养物质、代谢的运输,从而有利于骨组织的长入[4-6]。上述需求导致传统制造方法逐渐不能满足骨科植入物的发展要求。
金属增材制造技术的出现和发展为快速定制骨科植入物以及不同骨小梁多孔结构的精确成形提供了可能[7-9]。近年来,以电子束粉末床熔融技术(electron beam powder bed fusion, EB-PBF)和激光粉末床熔融技术(laser powder bed fusion, L-PBF)为代表的粉末床熔融技术(powder bed fusion,PBF)是应用最为广泛的金属增材制造技术[10-13]。该技术以电子束或激光束为能量源,根据零件的三维模型,基于离散-堆积的成形原理,逐点、逐线以及逐层熔化,最终实现金属零件的快速、精准制造。PBF技术可以根据植入物使用场景的不同,通过调整模型和制造工艺参数,快速制造出不同孔形貌、不同杆筋直径、不同孔径以及不同孔隙率的骨小梁多孔结构,以满足力学性能和骨长入特性的适配[14-16]。相对于L-PBF技术,EB-PBF技术在真空环境下成形,具有能量密度高、能量利用率高、成形效率快、成形应力低、零件洁净度高等突出优点[17-18],首个获得欧盟、美国食品药品监督管理局以及中国药品监督管理局认证的增材制造骨科植入物就是采用该技术制备,该技术也是目前增材制造骨科植入物的主流制造技术。随着人工关节、脊柱带量采购政策的实施,具有批量化、低成本制造优势的EB-PBF骨科植入物将迎来更加广阔的应用前景,但同时也在制造成本、多孔结构设计和检测方法等方面面临着诸多挑战。本文将主要介绍EB-PBF技术特点、EB-PBF设备发展现状以及EB-PBF钛合金、多孔钽骨科植入材料的研究和应用进展,在此基础上,对该领域的发展中面临的问题进行总结,旨在推动EB-PBF骨科植入材料获得更多的关注及应用,并为新一代植入材料的开发提供参考和指导。
1、EB-PBF技术特点
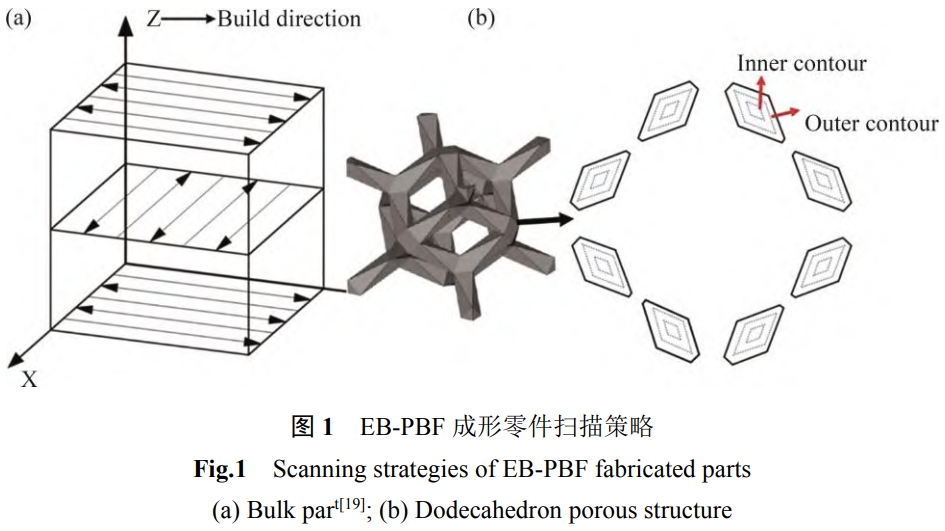
在EB-PBF实际成形前,首先需要将成形零件的三维数据模型沿高度方向按设定的层厚进行分层切片,获得每层二维截面信息,随后对二维截面信息进行扫描策略的设置。对于骨科植入物而言,致密部分和骨小梁多孔部分常采用不同的扫描策略。如图1(a)所示,致密部分常采用填充熔化的方式成形每层截面,该阶段电子束进行直线运动,具体为“蛇形扫描”的方式[19];对于骨小梁多孔部分而言,以点扫的方式对多孔杆筋的外轮廓和内轮廓进行熔化,轮廓线由间隔100μm的点组成。图1(b)所示为菱形十二面体多孔结构的扫描策略。在成形过程中,首先会根据成形材料的不同,利用电子束将底板加热至特定的温度,随后如图2所示,进行层层铺粉、粉床前预热、选区熔化、粉床后预热、底板下降,直至整个零件打印完成[17]。最后,将植入物毛坯取出,对多孔结构中未熔化的粉末进行清粉以及去除植入物的支撑,若植入物是纯多孔结构(如关节垫块),进行清洗、灭菌、包装后即可发往医院,若植入物包含实体结构(如髋臼杯),则需要对实体结构进行机加、抛光等后处理,再进行清洗、灭菌、包装。
由于能量源不同,EB-PBF与L-PBF相比具有如下特点:1)能量利用率高、功率大。各种金属材料对电子束有着稳定的高能量吸收率,对激光的能量吸收率则要低于电子束,并且与波长相关[20]。此外,市面上常用EB-PBF设备所用电子枪的功率为3~6kW,而常用L-PBF设备所用激光器的功率<1kW[21]。较高的能量利用率以及较大的单枪功率,使得EB-PBF成形过程中熔池较大、较深,电子束可以快速熔化粒径较粗的粉末,其常用的粉末粒径范围是45~105μm或45~150μm,大于L-PBF的15~45μm[22]。因此,EB-PBF成形过程中的层厚常设置在50μm、70μm甚至90μm,L-PBF层厚则多设置在20~30μm,这使得EB-PBF成形零件的速度要高于L-PBF技术。2)扫描速度快。由于使用磁场偏转,电子束的扫描速度最高可达8000 m/s,远高于使用机械振镜偏转的激光束,这使得EB-PBF成形过程中单层的熔化效率要高于L-PBF技术。3)成形应力低。基于较高的能量利用率、较大的功率以及大的扫描速度,在EB-PBF过程中,电子束可以实现对粉末床的快速预热,粉床最高预热温度可达1100℃,而L-PBF技术无法对粉床进行预热。首先,粉床的预热可以有效释放零件中的残余应力,成形零件无需进行热处理。其次,较低的残余应力导致EB-PBF成形过程中零件具有较低的变形倾向,在成形复杂结构零件时,只需要对零件添加防止移动的简单支撑,成形后手动去除支撑即可,而L-PBF需要添加强度较高的支撑,成形后需要通过线切割去除支撑。最后,粉床的预热可以使粉末具有一定的支撑作用,这有助于粉床上直接添加支撑,进而实现零件的叠层打印。4)真空环境成形。EB-PBF是在高真空下进行,这可以最大限度避免杂质元素的污染,适合活性材料及对氧敏感材料的成形。此外,真空环境下成形使得粉末单炉次使用的氧增量较低,有利于粉末的多次循环使用,降低零件制造过程中的原料成本。
然而,EB-PBF技术在加工骨科金属植入物也存在一些劣势。相对于激光光斑,电子束的光斑较大,加之使用的粉末较粗,使得EB-PBF的成形精度要低于L-PBF技术。此外,由于预热的存在,在EB-PBF成形多孔金属过程中,部分粉末会预烧结在杆筋上,给后续粉末去除带来困难。

2、EB-PBF设备的发展现状
相对于L-PBF,国内外从事EB-PBF技术和装备开发的单位较少。电子枪是EB-PBF设备的核心,不仅要具备大面积预热和精细扫描熔化的功能,还要兼顾长时间稳定运行的能力,直接决定着设备的成形尺寸、制造精度以及成形零件的质量及成形效率。与L-PBF设备的激光器不同,目前国内外尚无专用电子枪的商业化产品,各EB-PBF设备制造商在研制设备之前必须首先研发出专用电子枪。以W为阴极的直热式电子枪是第一代商业化EB-PBF设备使用的电子枪,具有成本低、性能稳定等优势,但在大功率下存在寿命短(<100h)、束斑直径大(200~300μm)等缺点。为了解决该问题,相关企业又推出了以单晶lab6为阴极的第二代直热式电子枪。相对于w阴极,lab6阴极具有寿命长(>500h)、功率大(6 kW)、束斑直径小(140μm)等优点,但该材质的阴极成本高,单根售价在1万~1.5万元之间,加之LaB6阴极易污染,对真空度要求较高,这也加大了电子枪的使用和维护成本。为了规避直热式电子枪的问题,我国西安赛隆增材技术股份有限公司采用间热式阴极原理,研发出了大功率、高精度、长寿命的低成本间热式电子枪。该间热式电子枪功率可达6kW,可快速将款幅面粉床预热至1 100℃并大幅提高打印效率。电子枪整体阴极组件使用寿命在400h以上,与直热式LaB6阴极的实际使用时间接近,满足大尺寸零件或长时间堆叠打印的制造需求。通过改变阴极的截面特性,使得高功率下的束斑直径可控,可实现宽幅域下束斑直径<100μm的精确扫描,满足零件高精度的制造需求。电子枪阴极与辅助阴极均采用W材质,耐造性好,成本不足直热式LaB6阴极的30%,满足零件低成本的制造需求。3种电子枪的优缺点如表1所列。
基于EB-PBF专用电子枪技术的发展,瑞典Arcam公司(现被美国GE公司收购)于2003年推出了世界上第一台商业化EB-PBF装备,针对不同的应用场景,该公司陆续推出了搭载直热式W阴极的A2X型设备以及搭载直热式LaB6阴极的Q10 Plus、Q20 Plus、SpectraL以及SpectraH型设备。西北有色金属研究院以及清华大学是国内最先从事EB-PBF技术和装备研发的单位,依托相关研究成果,西北有色金属研究院通过成果转化,成立西安赛隆增材技术股份有限公司,该公司推出了国内第一台商业化EB-PBF设备,并开发出多个型号搭载间热式W阴极的EB-PBF设备。清华大学则转化出天津清研智束科技有限公司,该公司现拥有4个型号的EB-PBF设备。此外,瑞典Freemelt公司、英国 Wayland Additive公司、日本JEOL公司、日本Tada Electric公司、德国Probeam公司、德国ALD公司也先后推出了EB-PBF设备[23],如表2所列。
表1 EB-PBF设备专用电子枪参数对比
Table 1 Parameter comparison of dedicated electron guns for EB-PBF equipment
| Cathode type | Max electron gun/kW | Minimum beam spot diameter/μm | Forming accuracy/mm | Filament life/h | Filament cost/¥ |
| Directly-heated tungsten cathode | 3 | 200-300 | ±0.2-0.3 | <100 | <100 |
| Directly-heated LaB6 cathode | 6 | 140 | ±0.2 | >500 | 10000-15000 |
| Indirectly-heat tungsten cathode | 6 | <100 | ±0.1 | >400 | >400 |
表2 EB-PBF设备生产厂商及设备型号[23]
Table 2 Manufacturers and equipment models of EB-PBF devices[23]
| Company | Model | Maximum bulid size/mm | Cathode type |
| Arcam | A2X | 200x200x380 | Directly-heated tungsten |
| Q10 plus | 200x200x200 | Directly-heated LaB6 | |
| Q20 plus | ∅350x380 | Directly-heated LaB6 | |
| Spectra L | ∅350x430 | Directly-heated LaB6 | |
| Spectra H | 250x430 | Directly-heated LaB6 | |
| Sailong AM | Y150 | 150x150x180 | Directly-heated tungsten |
| Y150 plus | 170x170x180 | Indirectly-heated tungsten | |
| T200 | 200x200x450 | Indirectly-heated tungsten | |
| H400 | 400x400x400 | Indirectly-heated tungsten | |
| Qbeam | E200 | 200x200x240 | Directly-heated tungsten |
| S200 | 200x200x240 | Directly-heated LaB6 | |
| S350 | 350x350x700 | Directly-heated LaB6 | |
| G350 | 350x350x700 | Directly-heated LaB6 | |
| Qbeam | S600 | 600x600x700 | Directly-heated LaB6 |
| Freemelt | Freemelt one | 100x100 | Directly-heated tungsten |
| Wayland Additive | Calibur3 | 300x300x450 | Directly-heated LaB6 |
| JEOL | JAM-5200EBM | 250x400 | Directly-heated LaB6 |
| Probeam | EBM30S | 300x300x400 | |
| TADA | EZ300 | 220x220x300 | Directly-heated LaB6 |
| ALD | EBuild 850 | 850x850x1000 |
3、EB-PBF钛合金骨科植入物的应用进展
作为骨科植入物使用范围最广、用量最大的金属材料,Ti-6Al-4V合金具有密度低、比强度高、耐蚀性能好、生物相容性好等特点[24]。
3.1 EB-PBF钛合金的组织及力学性能
对于骨科植入材料而言,严格控制内部缺陷十分重要,缺陷会严重影响植入物的力学性能,给初期及远期使用带来风险,其中不合适的工艺参数及粉末内部缺陷是造成植入物内部缺陷的主要原因。GALARRAGA等[25]发现EB-PBF技术成形的Ti-6Al-4V合金存在的主要缺陷为孔隙,孔隙主要分平行于扫描层方向的不规则形状孔隙(见图3(a))和球形孔(见图3(b))。不规则孔往往出现于未熔颗粒附近,当能量密度不足时合金中存在未熔颗粒,伴随着不规则孔隙的产生;球形孔则是气雾化粉末内部气体在成形过程中来不及溢出形成的。在Ti-6Al-4V合金的熔化过程中,熔化电流以及扫描速度是决定成形过程中能量密度的关键,随着熔化电流的增加以及扫描速度的减小,能量密度不断增加[26-27]。BAUEREISSB等[28]发现随着能量密度的增加,熔池流动力增大,EB-PBF Ti-6Al-4V合金熔合缺陷减小,致密度提高,试样表面的孔洞和块体中的不规则孔隙消失。然而,能量密度也不是越大越好,较大的能量密度会使得Ti-6Al-4V合金晶粒粗大,并且会导致植入物出现翘曲、鼓包等变形。
EB-PBF成形Ti-6Al-4V的显微组织如图4所示,沉积态的典型组织为沿建造方向贯穿多个粉层厚度的柱状原始β晶粒形貌。在合金顶层,有大量针状马氏体α'组织,同时观察到块状相(αm)[29]。EB-PBF成形过程中无扩散马氏体相变(β→α')、短程扩散块状相变(β→αm)以及长程扩散型相变(β→α+β)均可发生。当Ti-6Al-4V合金粉末熔化后,微观组织演变过程为L→β→α'+α+β→β→α'+α+α+β。当熔化成形当前粉层时,马氏体相变首先发生。在随后层的成形过程中,马氏体组织受循环热处理而重新进入β相区,随后经长程扩散型相变(包括马氏体分解)转变为α+β组成的经典网篮组织或魏氏组织,或短程扩散相变转变为块状组织。EB-PBF工艺参数显著影响着钛合金的组织,EVERHART等[30]发现,扫描线长度会对钛合金组织造成影响,随扫描长度增加,α+β板条宽度减小。GUO等[3]发现,随着熔化电流的增大以及扫描速度的减小,EB-PBF钛合金中的针状α'相晶粒尺寸变大。葛文君等[31]发现,随能量密度增加,位于试样顶部的马氏体区域由7~8个层厚增加到了22~25个层厚。
表3所列为EB-PBF技术成形Ti-6Al-4V合金的拉伸性能[32-35]。可以看出,EB-PBF Ti-6Al-4V合金的拉伸性能达到了YY/T0117.1一2024标准的要求,但是受内部缺陷、组织及氧含量等因素的影响,Ti-6Al-4V合金的拉伸性能分散性较大。由于柱状晶的存在,EB-PBF钛合金的拉伸性能呈现出各向异性[36-37],即沿竖直方向的抗拉强度要高于沿水平方向的抗拉强度,伸长率则低于水平方向。基于工艺参数对缺陷、晶粒尺寸的影响规律,其也进一步影响着Ti-6Al-4V合金的力学性能。当能量密度较低时,Ti-6Al-4V合金致密度较低,此时残余孔隙主导合金的力学性能,在应力的作用下,容易引起应力集中及参与孔隙桥接,导致合金过早断裂;当能量密度适当时,Ti-6Al-4V合金的致密度>99%,合金力学性能的主要影响因素由残余孔隙转变为晶粒尺寸、位错亚结构等;能量密度过高时,合金晶粒尺寸变大,导致强度降低,伸长率增大。


表3 EB-PBF Ti-6Al-4V合金的拉伸性能
Table 3 Tensile properties of Ti-6Al-4V alloy fabricated by EB-PBF
| Building direction | Tensile yield strength/MPa | Tensile strength/MPa | Elongation/% | Mass fraction of oxygen /% | Forming machine | Ref. |
| Vertical | 870.0 | 970.0 | 15.0 | 0.097 | Arcam A1 | [32] |
| Horizontal | 971.1 | 1 036.1 | 14.5 | 0.100 | Arcam A1 | [33] |
| Vertical | 973.0 | 1032.0 | 15.0 | Arcam Q10 | [34] | |
| Horizontal | 1051.0 | 1116.0 | 12.0 | Arcam Q10 | [34] | |
| Vertical | 1031.0 | 946.0 | 16.0 | 0.100 | Sailong Y150 | |
| Horizontal | 1046.0 | 962.0 | 14.5 | 0.100 | Sailong-Y150 | |
| Vertical | 996.3 | 12.7 | 0.108 | QEBMS200 | [35] | |
| YY/T 0117.1-2024 | 860.0 | 780.0 | 10.0 | <0.200 |
3.2 EB-PBF多孔钛合金的力学性能
借助于增材制造自由设计的特点,参照人骨的孔结构参数设计出的多孔钛合金支架一直是近年来的研究热点。除了避免“应力屏蔽”、有利于细胞生长和骨组织长入外,多孔结构还使得植入物表面具有较高的摩擦因数,保证了假体植入后的初期稳定性[38-39], EB-PBF技术使用的粉末的粒度大于L-PBF使用的粉末,成形过程中的“台阶”效应更加明显,这会进一步增大杆筋的表面粗糙度。图5所示为 EB-PBF技术可成形的常见孔结构单元,其快速扫描、低成形应力的特点使其在成形骨小梁结构时不受结构的限制[40]。常见多孔结构的压缩应力-应变曲线如图6所示[41-42]。EB-PBF多孔钛合金的压缩应力-应变曲线可分为3个阶段,即线性阶段、应力平台阶段以及致密阶段。在线性阶段,多孔钛合金支架的应力-应变曲线为一条直线,该阶段多孔支架的弹性模量与直线的斜率密切相关,多孔支架的杆筋发生压缩弯曲或压缩拉伸;在应力平台阶段,不断发生杆筋的屈服变形、弯曲变形和断裂,部分结构还出现单元胞的坍塌现象,应力-应变曲线上表现为曲线的不断波动,在该阶段多孔支架已失效;在致密阶段,钛合金支架不断被压实,应力-应变曲线不断上升。图7为不同密度的菱形十二面体 Ti-6Al-4V支架的压缩应力-应变曲线和 1000万次循环周期对应的压缩疲劳强度[43]。在孔结构相同时,多孔 Ti-6Al-4V支架的力学性能与密度的指数式呈线性关系,具体符合 Gibson-Ashby公式[44]:
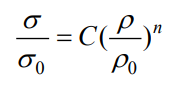
式中:σ代表多孔支架的强度,σ0代表致密材料的强度,ρ代表多孔支架的密度,ρ0代表致密材料的密度,C代表比例常数,n是指数。 n的理想值为1.5,但实际会偏大,这是由于 Ti-6Al-4V杆筋中存在成形缺陷,多孔支架实际强度低于理论值所致。
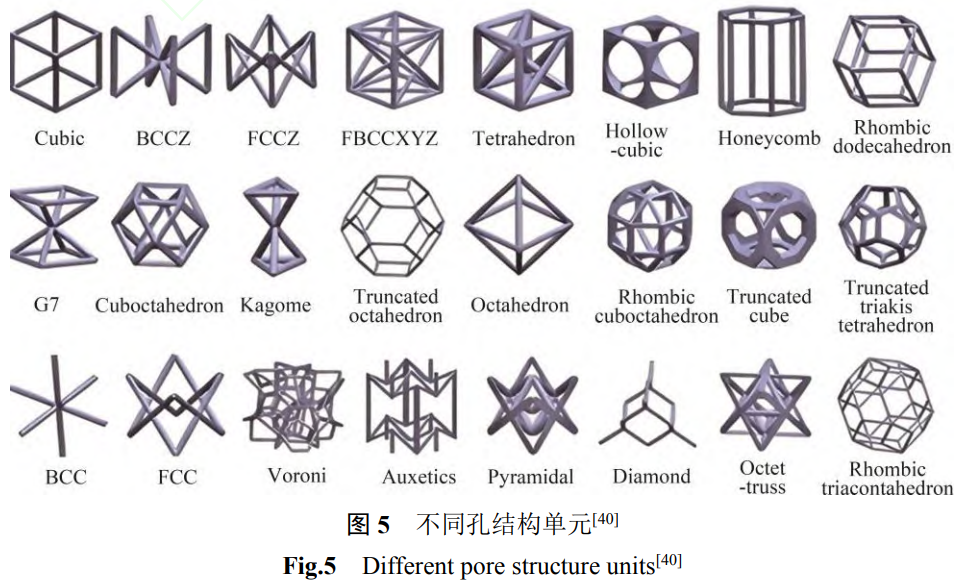
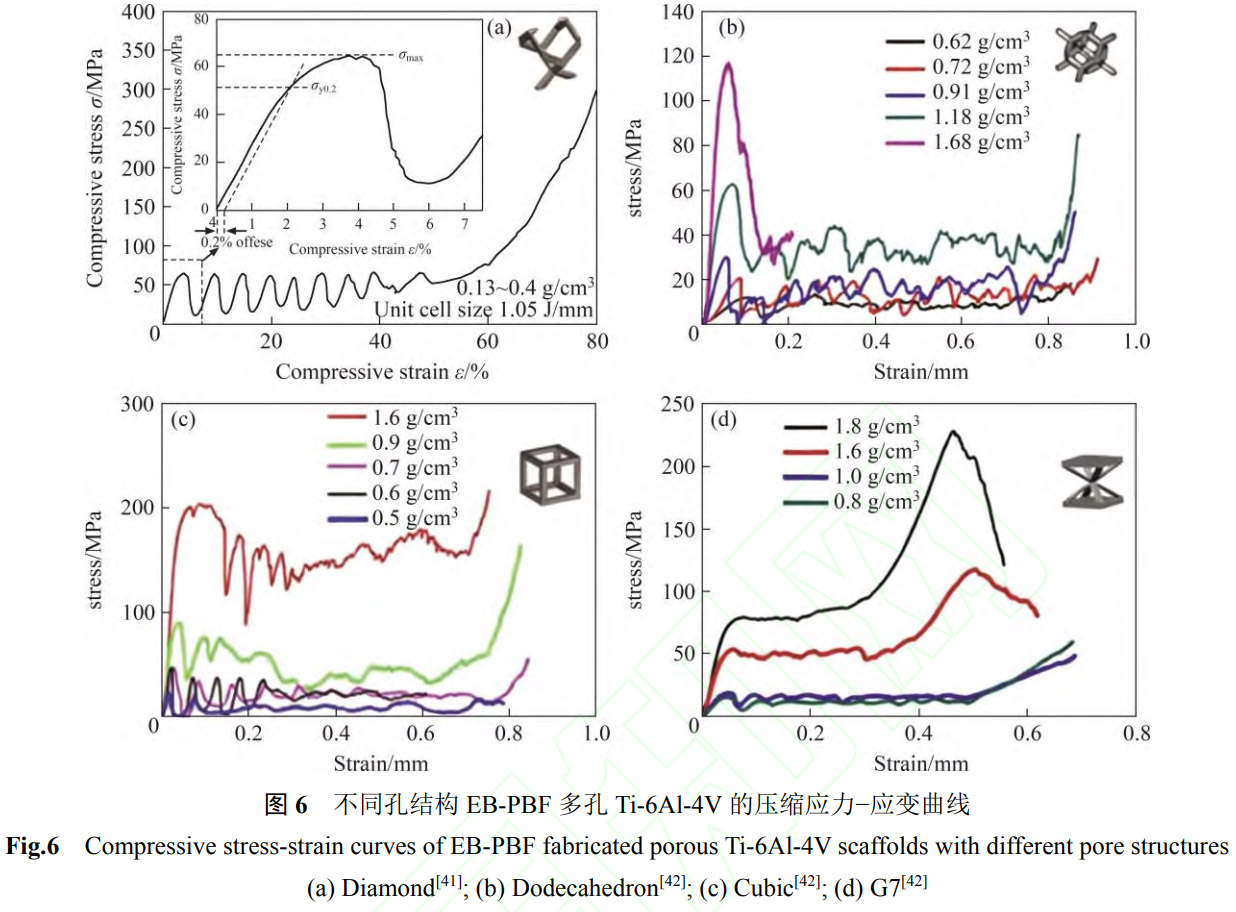
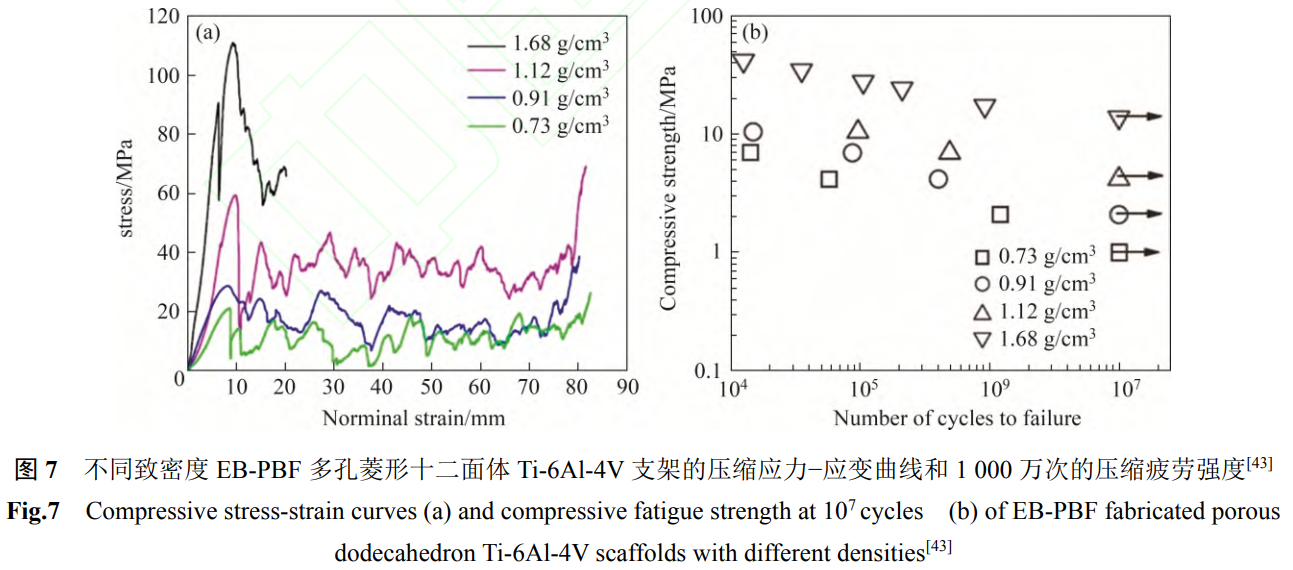
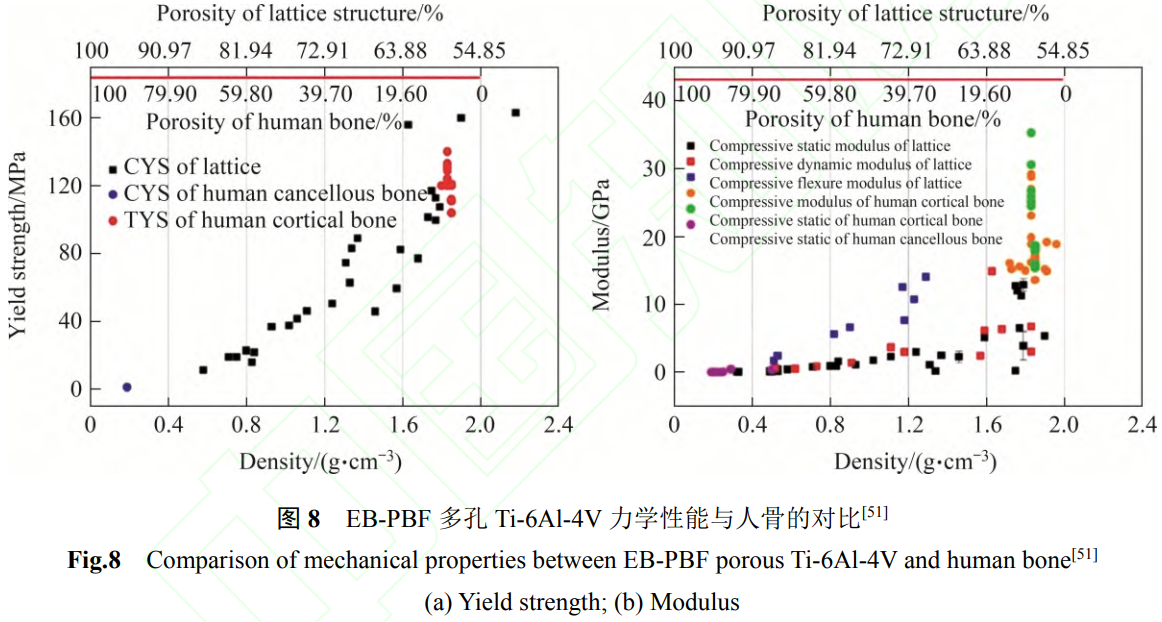
表4总结了不同孔结构EB-PBF多孔Ti-6Al-4V的力学性能[41-42,45-50]。可以看到,不同孔结构多孔Ti-6Al-4V支架的力学性能相差较大,一方面与孔结构参数相关,另一方面与所用粉末的氧含量也密切相关。图8所示为EB-PBF多孔Ti-6Al-4V与人骨屈服强度和模量的对比[51],结合表4以及其他关于人骨力学性能的报导[52],通过孔隙率和孔形貌的调节,可以使EB-PBF多孔Ti-6Al-4V支架的模量与人体松质骨的模量相当,但远低于人体皮质骨,这表明EB-PBF多孔Ti-6Al-4V作为骨植入材料是满足要求的,当与实体相结合时,制作的关节假体的力学性能可以作为承力部件进行使用。
表4不同孔结构多孔Ti-6Al-4V支架的力学性能
Table 4 Mechanical properties of porous Ti-6Al-4V scaffolds fabricated by EB-PBF
| Pore structure | Porosity/% | Elastic modulus/GPa | Compressive yield strength/MPa | Compressive strength/MPa | Tensile strength/MPa | Compressive fatigue strength/MPa |
| Cubic[45] | 80.0 | 1.60 | 22.0 | 29.3 | ||
| Cubic[46] | 60.7 | 194.6 | 89.9 | |||
| Diamond[41] | 60.0-87.0 | 0.40-6.50 | 11.4-99.7 | 16.3-118.8 | ||
| Diamond[50] | 60.0-83.0 | 19.1-112.7 | 4.8-16.9 at 10^6 cycles | |||
| Dodecahedron[42] | 58.0-88.0 | 0.50-6.50 | 10.0-100.0 | |||
| G7[42] | 58.0-88.0 | 0.50-5.00 | 8.0-80.0 | |||
| Gyroid[47] | 82.0 | 0.64 | 13.1 | 24.4 | ||
| Gyroid[48-49] | 84.0 | 0.45 | 14.6 | 3.1 at 10^6 cycles | ||
| Hexagonal[46] | 62.8 | 179.5 | 90.6 | |||
| Tetrahedron[46] | 58.5 | 90.2 | 59.2 |
3.3 EB-PBF钛合金骨科植入物的应用
我国在EB-PBF钛合金骨科植入物的应用方面与国外基本保持同步。表5所列为截止2024年12月已获得国家药品监督管理局(national medical products administration, NMPA)认证的增材制造骨科植入物。从表中可以看出,已有7家公司的27个EB-PBF钛合金骨科植入物获批上市,产品包括髋臼杯、椎间融合器、人工椎体、关节垫块等,产品采用的原料、设备、工艺也从之前的依赖进口到目前的国产化替代。2023年8月,西安赛隆增材技术股份有限公司助力迈瑞骨科“髋臼杯系统”通过NMPA审批(图9(a)),这是我国首个采用国产EB-PBF设备、原料及工艺取得三类医疗器械注册证的骨科植入产品。随后,西安赛隆增材技术股份有限公司先后助力迈瑞骨科采用EB-PBF技术制造的“椎间融合器”(图9(b))、“自稳型融合器”、“人工椎体”获得三类医疗器械注册证。随着EB-PBF设备和技术的不断成熟,加上国内无临床同品种比对取证政策的实施,基于骨小梁结构较好的临床应用效果,越来越多的医疗器械公司开始启动EB-PBF钛合金骨科植入物注册取证。EB-PBF技术拥有L-PBF技术不具备的叠层打印以及真空环境下粉末氧增量小、粉末可循环使用次数多的优势,这使得该技术在生产骨科植入物时生产效率高、生产成本低,有利于推动EB-PBF钛合金植入物批量的商业化应用。我国西安赛隆增材技术股份有限公司近年来瞄准EB-PBF骨科植入物的应用场景,利用自主知识产权的EB-PBF设备,建立起了年产能10万件的EB-PBF钛合金骨科植入物生产线,如图10(a)和(b)所示。2024年7月至2025年6月,该公司累计为10余家医疗器械公司生产了近2万件增材制造钛合金骨科植入物毛坯件,包括髋臼杯、椎间融合器、膝关节垫块、髋关节垫块、人工椎体等,图10(c)所示为其T200设备叠层打印的髋臼杯和椎间融合器,这显示着EB-PBF钛合金骨科植入物的商业化应用正向批量化逐步迈进。
表5 截止2024年12月已获得NMPA认证的增材制造骨科植入物
Table 5 Orthopedic implants fabricated by additive manufacturing certified by NMPA as of December 2024
| No. | Product | Company | Time | Method | Registration certificate |
| 1 | Hip joint prostheses Acetabular component | AK | 2015 | EB-PBF | 20153131311 |
| 2 | Vertebral prostheses | AK | 2016 | EB-PBF | 20163130859 |
| 3 | AVN Reconstruction system | AK | 2016 | EB-PBF | 20163131147 |
| 4 | Intervertebral cage | AK | 2016 | EB-PBF | 20163131289 |
| 5 | Lamina fixation plate system | AK | 2018 | EB-PBF | 20183130249 |
| 6 | Hip joint prostheses | JUST | 2019 | EB-PBF | 20193130509 |
| 7 | Pelvic defect matching prostheses | AK | 2020 | PBF | 20203130303 |
| 8 | Customized cervical fusion cage | AK | 2020 | EB-PBF | 20203130344 |
| 9 | Total knee prosthesis | AK | 2021 | EB-PBF | 20213130041 |
| 10 | Vertebral fusion cage | Huaxiang | 2021 | L-PBF | 20213130105 |
| 11 | Vertebral prosthesis | AK | 2021 | EB-PBF | 20213130426 |
| 12 | Intervertebral cage | AK | 2021 | EB-PBF | 20213130364 |
| 13 | Intervertebral cage | Norco | 2021 | EB-PBF | 20213130748 |
| 14 | Intervertebral cage | Huaxiang | 2022 | L-PBF | 20223130170 |
| 15 | Hip joint prostheses | iKey | 2022 | L-PBF | 20223130501 |
| 16 | Acetabular patch | Chunli | 2022 | EB-PBF | 20223130693 |
| 17 | Hip joint prostheses | Chunli | 2022 | EB-PBF | 20223131476 |
| 18 | Hip joint prostheses | LDK | 2022 | EB-PBF | 20223131529 |
| 19 | Intervertebral cage(Ta) | Huaxiang | 2023 | L-PBF | 20233130022 |
| 20 | Tibial plateau | AK | 2023 | EB-PBF | 20233130026 |
| 21 | Intervertebral cage | AK | 2023 | L-PBF | 20233130141 |
| 22 | Intervertebral cage | AK | 2023 | EB-PBF | 20233130206 |
| 23 | Thoracolumbar fusion matching prosthesis | AK | 2023 | PBF | 20233130524 |
| 24 | Vertebral prosthesis | LIBEIER | 2023 | EB-PBF | 20233130544 |
| 25 | Matching artificial vertebral body | We-do | 2023 | L-PBF | 20233130632 |
| 26 | Femoral head necrosis reconstruction rod | LIBEIER | 2023 | EB-PBF | 20233130744 |
| 27 | Long bone defect matching prosthesis | AK | 2023 | PBF | 20233130432 |
| 28 | Intervertebral cage | LIBEIER | 2023 | EB-PBF | 20233131102 |
| 29 | Intervertebral cage | SANYOU | 2023 | L-PBF | 20233131144 |
| 30 | Intervertebral cage | We-do | 2023 | L-PBF | 20233131348 |
| 31 | Acetabular cup system | Mindray | 2023 | EB-PBF | 20233131002 |
| 32 | Intervertebral cage | Chunli | 2023 | EB-PBF | 20233130955 |
| 33 | Vertebral prosthesis | Chunli | 2023 | EB-PBF | 20233131609 |
| 34 | Acetabular cup | Chunli | 2023 | EB-PBF | 20233131783 |
| 35 | Acetabular patch(Ta) | Huaxiang | 2023 | L-PBF | 20233131806 |
| 36 | Artificial vertebral body | Norco | 2023 | EB-PBF | 20233131673 |
| 37 | Cervical intervertebral cage system | Huaxiang | 2024 | L-PBF | 20243130936 |
| 38 | Intervertebral cage(Ta) | Dazhou | 2024 | L-PBF | 20243132044 |
| 39 | Hip head necrosis reconstruction rod(Ta) | Dazhou | 2024 | L-PBF | 20243130347 |
| 40 | Hip joint prostheses | Irene | 2024 | EB-PBF | 20243130115 |
| 41 | Intervertebral cage | Arign | 2024 | L-PBF | 20243132079 |
| 42 | Cervical intervertebral cage | SANYOU | 2024 | PBF | 20243131337 |
| 43 | Intervertebral cage | Norco | 2024 | EB-PBF | 20243131995 |
| 44 | Intervertebral cage | Ruiyi | 2024 | L-PBF | 20243132250 |
| 45 | Intervertebral cage | iKey Medical | 2024 | L-PBF | 20243130939 |
| 46 | Artificial vertebral body | Double | 2024 | PBF | 20243132190 |
| 47 | Intervertebral cage | Double | 2024 | L-PBF | 20243130624 |
| 48 | Matching knee joint prosthesis | Naton | 2024 | L-PBF | 20233131698 |
| 49 | Reconstruction-type acetabular system | JUST | 2024 | EB-PBF | 20243132547 |
| 50 | Intervertebral cage | SANYOU | 2024 | L-PBF | 20233131144 |
| 51 | Intervertebral cage | Mindray | 2024 | EB-PBF | 20243132565 |


4、EB-PBF多孔钽骨科植入物的研发进展
多孔钽具有优异的生物相容性、耐腐蚀性、骨传导性、骨诱导性和良好的力学性能,增材制造多孔钽是医学界和工程界近年来关注的热点[6,53-54]。
4.1 EB-PBF钽的组织及力学性能
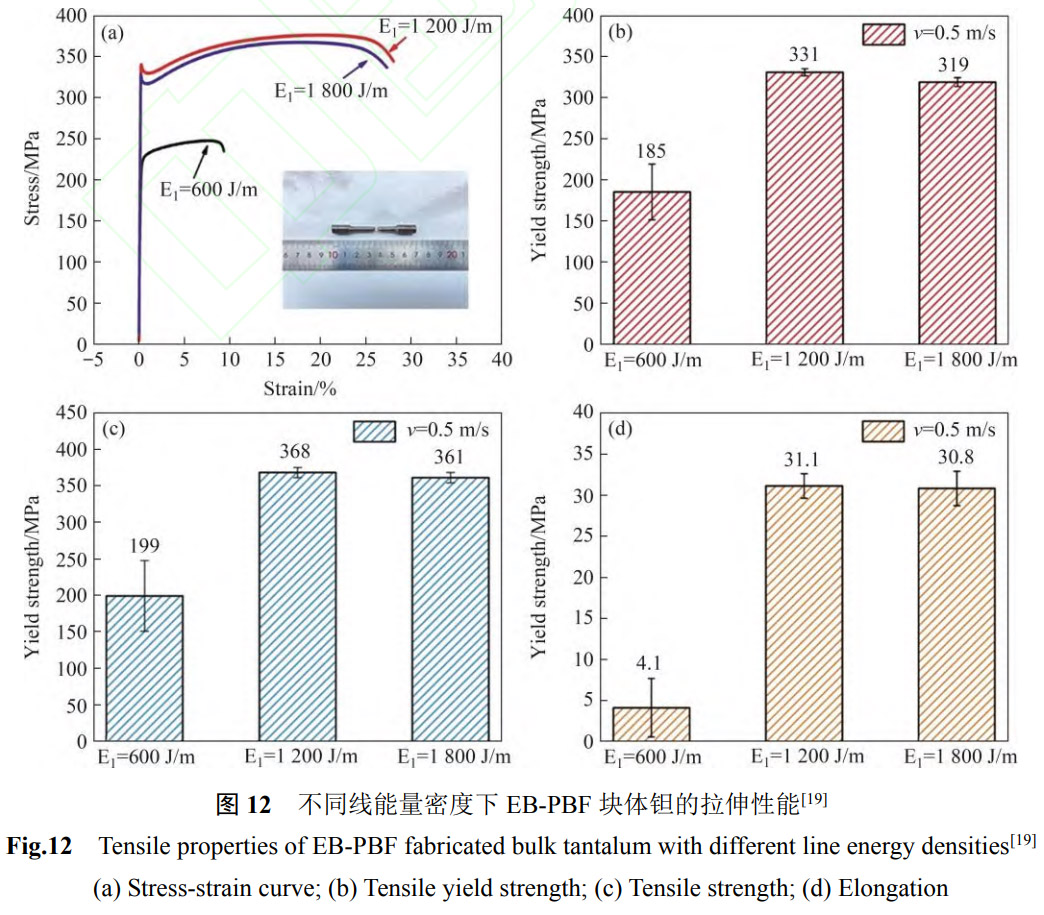
图11所示为EB-PBF钽的反极图[19]。可以看出,与EB-PBF钛合金类似,沿成形方向外延生长的柱状晶也普遍存在于金属钽中。随着线能量密度的增加,钽的内部缺陷逐步减少,且晶粒尺寸逐步增大。与L-PBF技术制备的钽相比[55-56],EB-PBF的柱状晶也普遍存在于金属钽中。随着线能量密度由于前预热和后预热的存在,成形钽过程中粉床温度一直在700℃以上,降低了温度梯度,使得钽粉熔化后的冷却速度低于L-PBF。图12所示为不同由于前预热和后预热的存在,成形钽过程中粉床温度一直在700℃以上,降低了温度梯度,使得钽粉熔化后的冷却速度低于L-PBF。图12所示为不同的线能量密度下,EB-PBF钽的拉伸应力-应变曲线和拉伸性能[19]。当线能量密度为1 200 J/m时,EB-PBF钽具有最优的拉伸性能,拉伸屈服强度达到331MPa,伸长率达到31.1%。在粉末氧含量差异不大的前提下,相对于L-PBF技术,EB-PBF钽的强度较低,伸长率较高,这也是基于EB-PBF钽较大的晶粒尺寸,使得晶界数量减少,位错可动距离长,从而获得较高的伸长率[57]。

4.2 EB-PBF多孔钽的力学性能
对比图12以及表4,EB-PBF钽的强度低于Ti-6Al-4V,但却具有更高的模量[58],要使得多孔钽植入物强度满足临床力学使用需求,避免“应力屏蔽”现象,孔结构的设计就十分重要,其显著影响着多孔钽的模量、强度及变形行为[59]。图13所示为不同孔结构多孔钽的压缩、拉伸以及弯曲应力-应变曲线[60]。在压缩试验中,G7和简单立方结构的多孔钽支架以杆筋的屈服变形为主,而菱形十二面体支架以弯曲变形为主,导致菱形十二面体多孔钽支架的抗压强度较低。但菱形十二面体多孔钽支架具有较好的拉伸和弯曲性能。在拉伸和弯曲变形中,菱形十二面体多孔钽支架的最大应力分布均匀,均匀的结构变形使得杆筋断裂延缓;而G7和简单立方结构多孔钽支架由于应力集中在横杆上,变形初期即出现杆筋断裂。基于不同的变形行为,70%孔隙率的EB-PBF菱形十二面体、G7和简单立方结构多孔钽的抗压强度依次降低。与L-PBF多孔钽相比[61],EB-PBF多孔钽具有更好的延展性,其在弯曲过程中杆筋断裂时的应变较高,甚至出现弯曲不断裂的情况[62],这主要得益于EB-PBF成形的真空环境使得多孔钽的氧含量较低,多孔钽具有更加优异的延展性。图14所示为不同孔结构多孔钽压缩疲劳性能。从图看出,随循环周期增加,EB-PBF多孔钽的压缩疲劳强度和疲劳比(压缩疲劳强度/压缩平台强度)逐步下降。相同孔隙率下,菱形十二面体、G7以及简单立方结构在200万次循环周期下对应的压缩疲劳强度及疲劳比依次上升。表6所列为不同孔结构EB-PBF多孔钽的力学性能[60]。相同孔隙率下,多孔钽的模量和力学性能要低于多孔Ti-6Al-4V支架,但其依然介于人体皮质骨和松质骨之间,满足骨植入材料的使用需求。而且,由于钽较高的密度,为了保证植入物的质量不会太高,实际使用中很少会出现实体-多孔复合的钽植入物,多孔钽常以纯多孔结构的髋关节垫块、膝关节垫块等填充材料的方式进行使用,这也使得钽的使用场景要少于Ti-6Al-4V。
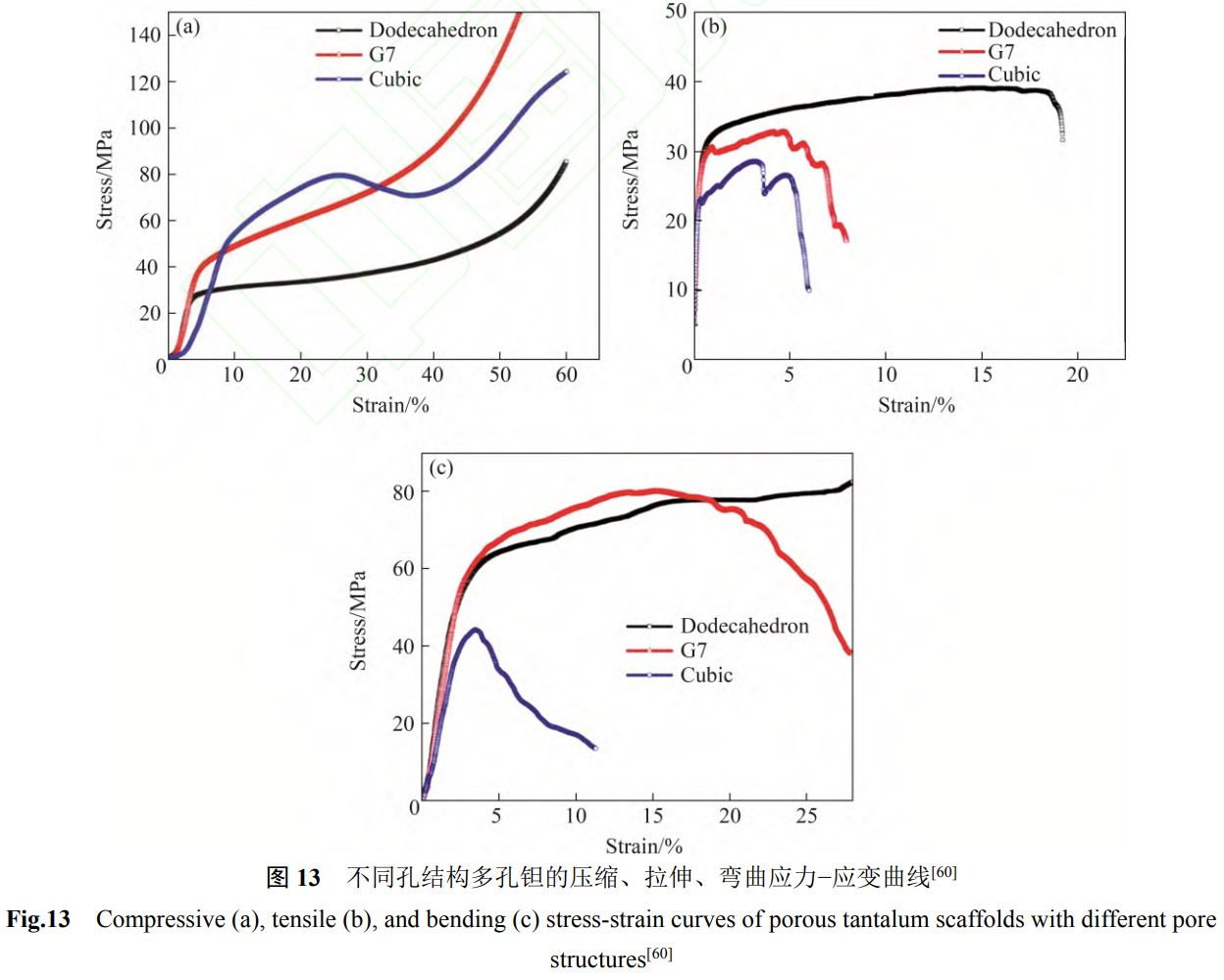
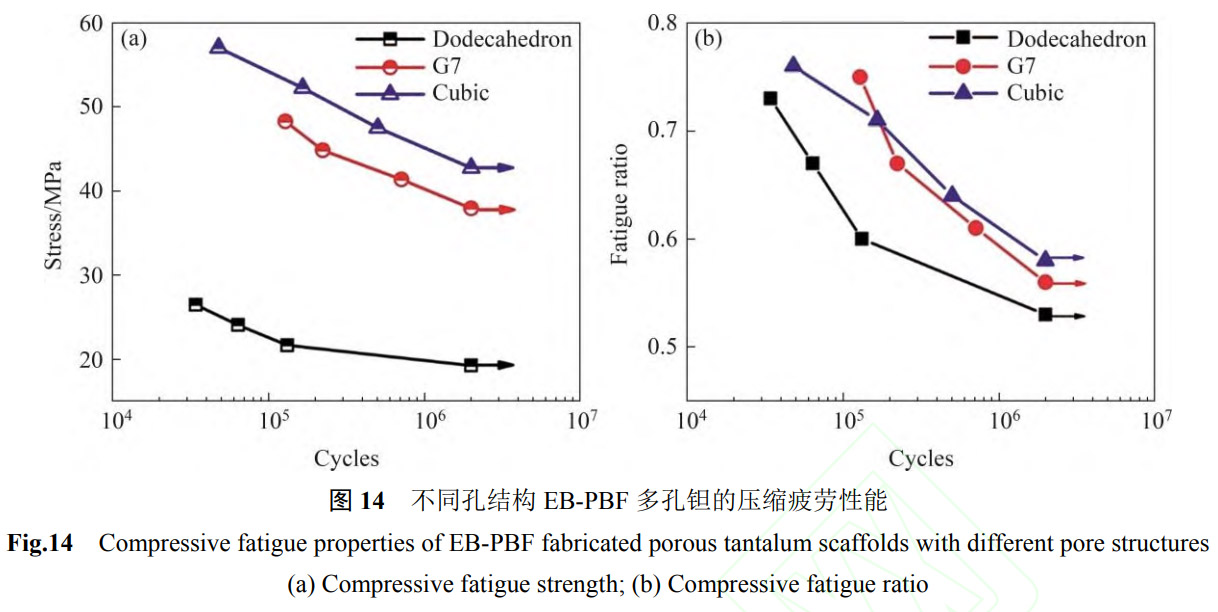
表6 70%孔隙率的EB-PBF多孔钽的力学性能[60]
Table 6 Mechanical properties of porous tantalum with the porosity of 70% fabricated by EB-PBF
| Pore structure | Elastic modulus/GPa | Compressive yield strength/MPa | Tensile yield strength/MPa | Bending yield strength/MPa | Compressive fatigue strength/MPa |
| Dodecahedron | 1.10 | 24.1 | 27.6 | 48.8 | 19.3 |
| G7 | 1.01 | 34.5 | 26.2 | 47.8 | 37.9 |
| Cubic | 0.93 | 47.5 | 18.4 | 31.0 | 42.8 |
4.3 EB-PBF多孔钽的临床试验
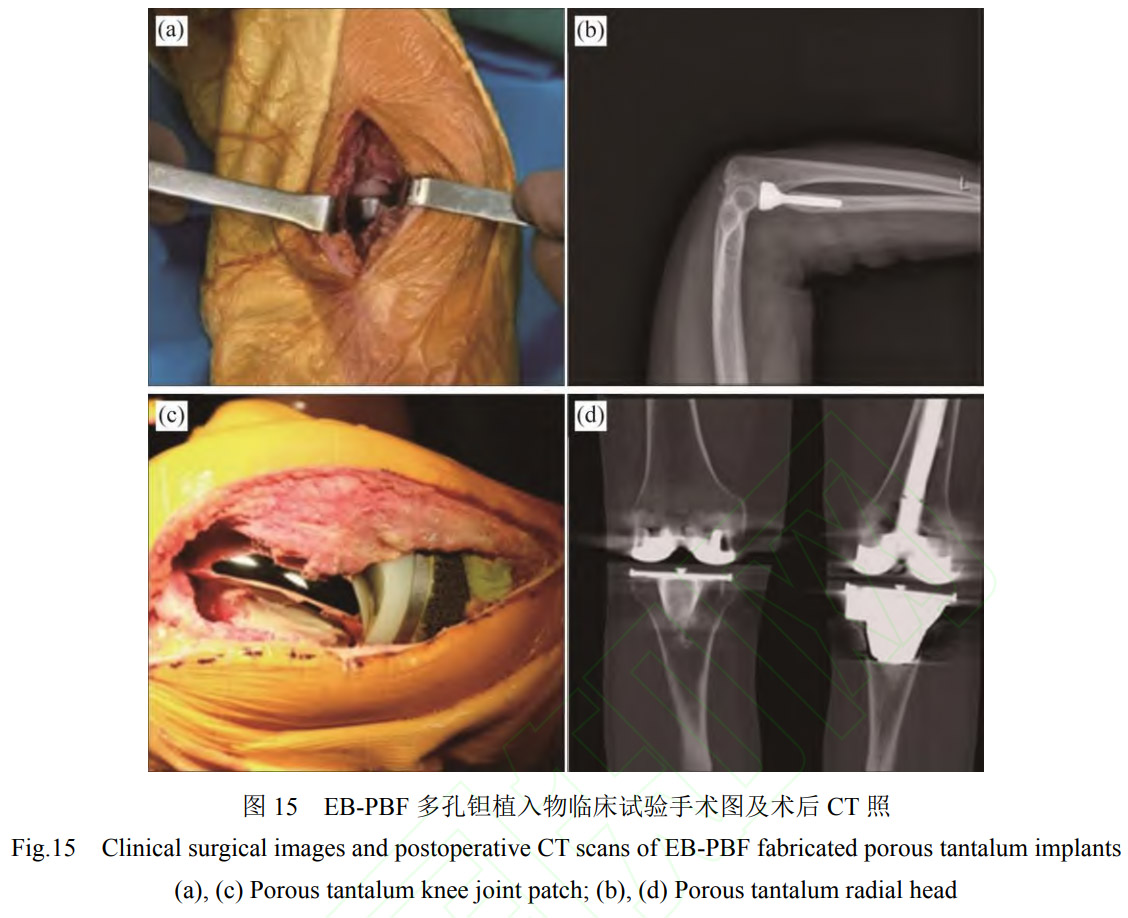
在临床试验方面,西安赛隆增材技术股份有限公司依托科技部国家重点研发计划项目“个性化多孔钽植入假体粉床电子束增材制造关键技术和临床应用”项目(2016YFB101400),累计完成100余例个性化多孔钽临床试验,患者年龄3~83岁,植入物包括多孔钽髋关节补块、膝关节补块、桡骨假体、舟骨假体等。如ZHANG等[63]利用EB-PBF多孔钽桡骨假体对7例桡骨头粉碎性骨折患者进行了桡骨头置换术,术后随访数据显示,患者术后疼痛减轻,肘关节功能改善,多孔钽假体展现出优异骨长入特性。AO等[64]观察了6例使用EB-PBF多孔钽膝关节补块进行全膝关节置换术翻修患者的恢复情况,其临床手术照片如图15所示,在术后26.3个月后,没有患者出现任何手术相关并发症,植入关节内的多孔钽假体稳定,骨缺损得到有效重建,患者膝关节功能得到明显改善。
5、EB-PBF骨科植入材料的机遇和挑战
除了钛合金和钽之外,增材制造锆铌合金也是临床上较为关注的硬组织植入材料。锆铌合金具有优异的生物相容性、良好的耐腐蚀性、适配的力学性能以及较低的密度[65-66]。利用该材料的氧化特性,经过原位氧化工艺可以在锆铌合金表面形成一层致密的氧化锆陶瓷膜,使得该材料制成的假体兼具金属的抗断裂韧性和陶瓷的耐磨性[67]。利用增材制造一体成形的特点,可以制备兼具耐磨性和骨长入特性的双功能界面假体(见图16),这使得其在关节面假体上有较好的应用。相对于钛合金和钽,增材制造锆铌合金的研究较为滞后,未见相关原料、工艺及临床试验的报导。随着技术和设备的不断发展,EB-PBF技术成形的骨科植入物逐步被医患所认知和接受。然而,要想像传统制造技术那样获得大规模使用,依然面临以下几个问题需要解决。

1)制造成本。随着关节、脊柱带量采购政策的落地,医疗器械公司对于植入物的制造成本十分敏感。基于EB-PBF技术叠层打印的成形方式以及较低的钛合金粉末成本,使得EB-PBF钛合金植入物的成本已与传统机加+喷涂技术制备的植入物相当,这也是其如今批量使用的主要原因。然而,对于多孔钽和锆铌合金等新材料而言,其较高的粉末制造成本以及因为增材制造过程中氧含量的不断增加导致粉末循环使用次数的限制,使得增材制造多孔钽、锆铌合金骨科植入物的成本极高,大大限制了其进一步商业化推广应用。因此,钽、锆铌等新材料球形金属粉末低成本制造技术以及植入物批量生产过程中粉末循环使用准则的制定十分必要。
2)多孔结构设计。增材制造技术与传统制造技术在骨科植入物制造上最大的区别就是其可以一体制造出不同的骨小梁多孔结构,以便于骨组织的充分生长。基于电子束快速扫描的特点,目前已报导的EB-PBF技术可以成形上百种多孔结构。然而,实际应用于临床或者骨科植入物产品开发的孔结构十分有限。现有研究多聚焦于标准试样孔形貌、孔隙率、孔径等孔结构参数对力学性能以及骨长入特性的基础研究,缺乏针对具体应用场景的适配性设计及产品研究。更关键的是,医工交互平台尚未成熟,临床医生对复杂孔结构的理解存在壁垒,导致设计成果难以转化为临床可用的标准化产品或定制化产品。因此,构建医工协同数据库、开发基于多孔结构的智能设计软件十分必要。
3)检测方法。作为典型的粉末床熔融技术,粉末的卫星粉、空心粉以及成形过程中工艺的不适配很容易在植入物中引入缺陷。除了明确粉末技术要求、建立粉末循环使用准则以及不同骨科植入物EB-PBF工艺规范外,通过后续检测的方式在增材制造工艺后将不合格品检出是目前常用的避免缺陷的方法。一方面,当前检测主要依赖CT扫描,虽能精准表征金属粉末内部气孔分布,但单件检测成本高达数千元,且耗时较长,难以满足规模化生产需求;另一方面,传统抽样检测方式存在漏检风险,这给临床应用带来了极大的风险。因此,寻找快速、低成本以及可靠的检测方法也是决定EB-PBF骨科植入物能否批量商业化应用的关键。
6、结语
随着设备与技术的不断成熟,EB-PBF技术制备的钛合金骨科植入物已获得规模化的商业应用,多孔钽、锆铌合金骨科植入物也展现出较好的临床应用前景。但现阶段,多孔结构设计壁垒、检测方法的缺失以及钽粉、锆铌粉较高的生产及使用成本,阻碍着EB-PBF骨科植入物的进一步发展,需要材料、设备供应商以及医疗器械公司、临床医生、政府监管部门共同协作和努力,推动EB-PBF技术乃至增材制造技术在骨科植入物领域的进一步发展,提升国民生命健康水平。
参考文献:
[1]尹浜兆,秦瑜,温鹏,等.激光粉末床熔融制备金属骨植入物[J].中国激光,2020,47(11):8-25.
YIN Bangzhao, QIN Yu, WEN Peng,et al. Laser powder bed fusion for fabrication of metal orthopedic implants[J].Chinese Journal of Lasers,2020,47(11):8-25.
[2]杨坤,汤慧萍,李元元.粉末床电子束3D打印医用金属材料的研究进展[J].功能材料,2020,51(3):3038-3046.
YANG Kun, TANG Huiping, LI Yuanyuan. Development and application of orthopaedic medical materials by selective electron beam melting processes[J]. Journal of Functional Materials,2020,51(3):3038-3046.
[3] GUO C, GE W J, LIN F. Effects of scanning parameters on material deposition during electron beam selective melting of Ti-6Al-4V powder[J]. Journal of Materials Processing Technology,2015,217:148-157.
[4]周银.基于骨长入模型的多孔植入物优化设计[D].南京:东南大学,2019.
ZHOU Yin. Optimization design of porous implant based on bone ingrowth model[D]. Nanjing: Southeast University,2019.
[5]CHENG A, HUMAYUN A, COHEN D J, et al. Additively manufactured 3D porous Ti-6Al-4V constructs mimic trabecular bone structure and regulate osteoblast proliferation,differentiation and local factor production in a porosity and surface roughness dependent manner[J]. Biofabrication,2014,6(4):045007.
[6]GAO H R, YANG J Z, JIN X, et al. Porous tantalum scaffolds: fabrication, structure, properties, and orthopedic applications[J]. Materials& Design, 2021, 210: 110095.
[7]CHEN L Y, LIANG S X, LIU Y J, et al. Additive manufacturing of metallic lattice structures: Unconstrained design, accurate fabrication, fascinated performances, and challenges[J]. Materials Science& Engineering R,2021,146:100648.
[8]杨坤,汤慧萍,王建,等.标准化和增材制造个性化多孔钽植入体的研究进展[J].热加工工艺,2017,46(22):5-8.
YANG Kun, TANG Huiping, WANG Jian, et al. Research development of standardized and additively manufactured custom-made porous tantalum implant[J]. Hot Working Technology,2017,46(22):5-8.
[9]汪小康,吴丽光,叶建波,等.选区激光熔化316L不锈钢梯度晶格结构的压缩性能[J].粉末冶金材料科学与工程,2025,30(5):446-455.
WANG Xiaokang, WU Liguang, YE Jianbo, et al.Compressive properties of selective laser melted 316L stainless steel gradient lattice structures[J]. Materials Science and Engineering of Powder Metallurgy, 2025, 30(5): 446-455.
[10] PONADER S, VAIRAKTARIS E, HEINL P, et al. Effects of topographical surface modifications of electron beam melted Ti-6Al-4V titanium on human fetal osteoblasts[J]. Journal of Biomedical Materials Research Part A, 2008, 84A(4):1111-1119.
[11] SARACYAKUPOGLU T. The qualification of the additively manufactured parts in the aviation industry[J]. American Journal of Aerospace Engineering, 2019,6(1): 1-10.
[12] RAMSPERGER M, EICHLER S. Electron beam based additive manufacturing of alloy 247 for turbine engine application: from research towards industrialization[J].Metallurgical and Materials Transactions A, 2023, 54(5):1730-1743.
[13]马悦,袁铁锤,黄洋,等.激光粉末床熔融304L不锈钢显微组织及力学性能各向异性[J].粉末冶金材料科学与工程,2025,30(4):364-377.
MA Yue, YUAN Tiechui, HUANG Yang, et al.Microstructure and anisotropic mechanical properties of laser powder bed fusion 304L stainless steel[J]. Materials Science and Engineering of Powder Metallurgy, 2025, 30(4):364-377.
[14] RADLOF W, POLLEY C, SEITZ H, et al. Influence of structure-determining parameters on the mechanical properties and damage behavior of electron beam melted lattice structures under quasi-static and fatigue compression loading[J]. Materials Letters,2021,289:129380.
[15] HUO P C,ZHAO Z Y,BAI P K,et al. Deformation evolution and fracture mechanism of porous TC4 alloy scaffolds fabricated using selective laser melting under uniaxial compression[J]. Journal of Alloys and Compounds, 2021,861:158529.
[16] AHMADI S M, YAVARI S A, WAUTHLE R, et al.Additively manufactured open-cell porous biomaterials made from six different space-filling unit cells: the mechanical and morphological properties[J]. Materials, 2015, 8(4):1871-1896.
[17]汤慧萍.粉末床电子束3D打印Ti-6Al-4V合金的工程应用技术研究进展[J].中国材料进展,2020,39(7):551-558.
TANG Huiping. Research progress on engineering application of Ti-6Al-4V alloy fabricated by selective electron beam melting process[J]. Materials China, 2020,39(7):551-558.
[18] ZHANG L C, LIU Y J, LI S J, et al. Additive manufacturing of titanium alloys by electron beam melting: a review[J].Advanced Engineering Materials,2018,20(5):1700842.
[19] GUO Y, CHEN C, WANG Q B, et al. Microstructural evolution and mechanical behavior of additively manufactured tantalum produced by electron beam powder bed fusion[J]. International Journal of Refractory Metals and Hard Materials,2023,110:106046.
[20]张靖.电子束选区熔化数字式扫描控制系统研究[D].北京:清华大学,2011.
ZHANG Jing. Research on digitized scanning control system for electron beam selective melting[D]. Beijing: Tsinghua University,2011.
[21]岳晓泽,魏恺文,刘宇光,等.高功率激光粉末床熔融成形GH4169高温合金的显微组织与力学性能研究[J].中国激光,2025,52(4):183-194.
YUE Xiaoze, WEI Kaiwen,LIU Yuguang, et al.Microstructure and mechanical properties of GH4169 superalloy via high-power laser powder bed fusion[J].Chinese Journal of Lasers, 2025, 52(4): 183-194.
[22] SRIVASTAVA M, RATHEE S, PATEL V, et al. A review of various materials for additive manufacturing: recent trends and processing issues[J]. Journal of Materials Research and Technology,2022,21:2612-2641.
[23] JIAO M H, LONG H Y, XIAO B W, et al. Electron beam powder bed fusion additive manufacturing: a comprehensive review and its development in China[J]. Additive Manufacturing Frontiers,2024,3(4):200177.
[24] YADROITSEV I, KRAKHMALEV P, YADROITSAVA I.Selective laser melting of Ti6Al4V alloy for biomedical applications: temperature monitoring and microstructural evolution[J]. Journal of Alloys and Compounds, 2014, 583:404-409.
[25] GALARRAGA H, LADOS D A, DEHOFF R R, et al.Effects of the microstructure and porosity on properties of Ti-6Al-4V ELI alloy fabricated by electron beam melting(EBM)[J].Additive Manufacturing,2016,10:47-57.
[26] SAMES W. Additive manufacturing of inconel 718 using electron beam melting: processing, post-processing,&mechanical properties[D]. Texas: Texas A&M University,2015.
[27] YANG K, WANG J, TANG H P, et al. Additive manufacturing of in-situ reinforced Ti-35Nb-5Ta-7Zr(TNTZ)alloy by selective electron beam melting(SEBM)[J]. Journal of Alloys and Compounds, 2020, 826: 154178.
[28] BAUEREISS BA, SCHAROWSKY T, KORNER C. Defect generation and propagation mechanism during additive manufacturing by selective beam melting[J]. Journal of Materials Processing Technology, 2014, 214(11): 2522-2528.
[29] LU S L, QIAN M, TANG H P, et al. Massive transformation in Ti-6Al-4V additively manufactured by selective electron beam melting[J]. Acta Materialia,2016,104:303-311.
[30] EVERHART W, DINARDO J, BARR C, et al. The effect of scan length on the structure and mechanical properties of electron beam-melted Ti-6Al-4V[J]. Metallurgical and Materials Transactions A, 2017, 48A(2): 697-705.
[31]葛文君,郭超,林峰.工艺参数对电子束选区熔化成形Ti6Al4V合金显微组织的影响[J].稀有金属材料与工程,2015,44(12):3215-3218.
GE Wenjun, GUO Chao, LIN Feng. Microstructures of Ti-6Al-4V components synthesized via electron beam selective melting[J]. Rare Metal Materials and Engineering,2015,44(12):3215-3218.
[32] TANG H P, QIAN M, LIU N, et al. Effect of powder reuse times on additive manufacturing of Ti-6Al-4V by selective electron beam melting[J]. The Journal of the Minerals,Metals& Materials Society,2015,67(3):555-563.
[33] SUN Y Y, GULIZIA S, FRASER D, et al. Layer additive production or manufacturing of thick sections of Ti-6Al-4V by selective electron beam melting(SEBM)[J]. The Journal of the Minerals, Metals& Materials Society, 2017, 69(10):1836-1843.
[34] ZHAI Y W, GALARRAGA H, LADOS D A. Microstructure evolution, tensile properties, and fatigue damage mechanisms in Ti-6Al-4V alloys fabricated by two additive manufacturing techniques[J]. Procedia Engineering, 2015,114:658-666.
[35]郭金鑫,于大千,阚文斌,等.控温策略优化对电子束选区熔化成形TC4钛合金力学性能的影响[J].材料研究与应用,2023,17(6):1015-1022.
GUO Jinxin, YU Daqian, KAN Wenbin, et al. Influence of temperature control strategy optimization on the mechanical properties of TC4 titanium alloy fabricated by electron beam selective melting[J]. Materials Research and Application,2023,17(6):1015-1022.
[36] BRUNO J, ROCHMAN A, CASSAR G. Effect of build orientation of electron beam melting on microstructure and mechanical properties of Ti-6Al-4V[J]. Journal of Materials Engineering and Performance,2017,26(2):692-703.
[37] EDWARDS P, O'CONNER A, RAMULU M. Electron beam additive manufacturing of titanium components: properties and performance[J]. Journal of Manufacturing Science and Engineering,2013,135(6):061016.
[38] WANG Y H, JING Z H, XU L, et al. Comparative effects of porous tantalum and porous titanium: a systematic review and meta-analysis[J/OL]. The Journal of Arthroplasty,[2026-03-02].https://doi.org/10.1016/j.arth.2025.09.024.
[39] SMITH J O, SENGERS B G, AARVOLD A, et al. Tantalum trabecular metal-addition of human skeletal cells to enhance bone implant interface strength and clinical application[J]. Journal of Tissue Engineering and Regenerative Medicine,2014,8(4):304-313.
[40] ZHONG H Z, SONG T T, LI C W, et al. The Gibson-Ashby model for additively manufactured metal lattice materials: its theoretical basis, limitations and new insights from remedies[J]. Current Opinion in Solid State and Materials Science,2023,27(3):101081.
[41] HEINL P, KORNER C, SINGER R F. Selective electron beam melting of cellular titanium: mechanical properties[J].Advanced Engineering Materials,2008,10(9):882-888.
[42] LI S J, XU Q S, WANG Z, et al. Influence of cell shape on mechanical properties of Ti-6Al-4V meshes fabricated by electron beam melting method[J]. Acta Biomaterialia,2014,10(10):4537-4547.
[43] LI S J, MURR L E,CHENG X Y,et al. Compression fatigue behavior of Ti-6Al-4V mesh arrays fabricated by electron beam melting[J]. Acta Materialia,2012,60(3):793-802.
[44] GIBSON L J, ASHBY M F. Cellular Solids: Structure and Properties[M]. Cambridge: Cambridge University Press,1997.
[45]HEINL P, MULLER L, KORNER C, et al. Cellular Ti-6Al-4V structures with interconnected macro porosity for bone implants fabricated by selective electron beam melting[J].Acta Biomaterialia,2008,4(5):1536-1544.
[46]张学哲.电子束选区熔化Ti-6Al-4V点阵材料成形能力及性能研究[D].沈阳:东北大学,2019.
ZHANG Xuezhe. Additive manufacturing of Ti-6Al-4V lattice materials by selective electron beam melting:manufacturability and properties[D]. Shenyang: Northeastern University,2019.
[47] ATAEE A, LI Y C, FRASER D, et al. Anisotropic Ti-6Al-4V gyroid scaffolds manufactured by electron beam melting(EBM) for bone implant applications[J]. Materials& Design,2018,137:345-354.
[48]YANEZ A,FIORUCCI M P,CUADRADO A,et al. Surface roughness effects on the fatigue behaviour of gyroid cellular structures obtained by additive by additive manufacturing[J].International Journal of Fatigue, 2020, 138: 105702.
[49] YANEZ A, CUADRADO A, MARTEL O, et al. Gyroid porous titanium structures: a versatile solution to be used as scaffolds in bone defect reconstruction[J]. Materials&Design,2018,140:21-29.
[50] HRABE N W, HEINL P, FLINN B, et al.Compression-compression fatigue of selective electron beam melted cellular titanium(Ti-6Al-4V)[J]. Journal of Biomedical Materials Research Part B: Applied Biomaterials,2011,99B(2):313-320.
[51] ZHANG X Z, LEARY M, TANG H P, et al. Selective electron beam manufactured Ti-6Al-4V lattice structures for orthopedic implant applications: current status and outstanding challenges[J]. Current Opinion in Solid State and Materials Science, 2018, 22(3): 75-99.
[52] ZHANG X Z, TANG H P, LEARY M, et al. Toward manufacturing quality Ti-6Al-4V lattice struts by selective electron beam melting(SEBM) for lattice design[J]. The Journal of the Minerals, Metals& Materials Society, 2018,70(9):1870-1876.
[53]杨柳,王富友.医学 3D打印多孔钽在骨科的应用[J].陆军军医大学学报,2019,41(19):1859-1866.
YANG Liu, WANG Fuyou. Progress of 3D printed porous tantalum in orthopedics[J]. Journal of Army Medical University,2019,41(19):1859-1866.
[54]赵德伟,李军雷.多孔Ta的制备及其作为骨植入材料的应用进展[J].金属学报,2017,53(10):1303-1310.
ZHAO Dewei, LI Junlei. Fabrication of the porous tantalum and its current status used as orthopedics implants materials[J].Acta Metallurgica Sinica,2017,53(10):1303-1310.
[55] ZHOU L B, CHEN J, LI C, et al. Microstructure tailoring to enhance strength and ductility in pure tantalum processed by selective laser melting[J]. Materials Science and Engineering A,2020,785:139352.
[56] SONG C H, DENG Z T, ZOU Z, et al. Pure tantalum manufactured by laser powder bed fusion: influence of scanning speed on the evolution of microstructure and mechanical properties[J]. International Journal of Refractory Metals and Hard Materials,2022,107:105882.
[57] ZHOU L B, YUAN T C, LI R D, et al. Selective laser melting of pure tantalum: densification, microstructure and mechanical behaviors[J]. Materials Science and Engineering A,2017,707:443-451.
[58] MARTIENSSEN W, WARLIMONT H. Springer Handbook of Condensed Matter and Materials Data[M]. Berlin:Springer,2005.
[59]杨景周,倪晓军,程豪,等.增材制造多孔钽骨科植入材料研究进展[J].稀有金属材料与工程,2026,55(3):808-829.
YANG Jingzhou, NI Xiaojun, CHENG Hao, et al. Research progress of additively manufactured porous tantalum orthopedic implantable material[J]. Rare Metal Materials and Engineering,2026,55(3):808-829.
[60] GUO Y, CHEN C, PAN Y M, et al. Influence of pore structures on deformation behavior and mechanical properties of porous tantalum scaffolds fabricated by electron beam powder bed fusion[J]. Transactions of Nonferrous Metals Society of China, 2023, 33(12): 3725-3738.
[61] YANG J Z, JIN X, GAO H R, et al. Additive manufacturing of trabecular tantalum scaffolds by laser powder bed fusion:mechanical property evaluation and porous structure characterization[J]. Materials Characterization, 2020, 170:110694.
[62] TANG H P, YANG K, JIA L,et al. Tantalum bone implants printed by selective electron beam manufacturing(SEBM)and their clinical applications[J]. The Journal of the Minerals,Metals& Materials Society, 2020, 72(3): 1016-1021.
[63] ZHANG C G, CHEN H, FAN H Q, et al. Radial head replacement using personalized 3D printed porous tantalum prosthesis[J]. Journal of Materials Research and Technology,2022,20:3705-3713.
[64] AO Y N, GUO L, CHEN H, et al. Application of three-dimensional-printed porous tantalum cones in total knee arthroplasty revision to reconstruct bone defects[J].Frontiers in Bioengineering and Biotechnology, 2022, 10:925339.
[65]吴妍贝.锆铌合金单髁假体生物力学研究[D].天津:天津理工大学,2025.
WU Yanbei. Biomechanical study of zirconium-niobium alloy unicondylar prosthesis[D]. Tianjin: Tianjin University of Technology,2025.
[66]吴妍贝,郝溥俊,高丽兰,等.骨-多孔锆铌合金假体界面应力分析[J/OL].天津理工大学学报,[2026-01-29].https://link.cnki.net/urlid/12.1374.N.20250123.1452.006.
WU Yanbei, HAO Fujun, GAO Lilan, et al. Stress analysis of the bone-porous zirconium-niobium alloy prosthesis interface[J/OL]. Journal of Tianjin University of Technology,[2026-01-29]. https://link.cnki.net/urlid/12.1374.N.20250123.1452.006.
[67] HOFER J K, EZZET K A. A minimum 5-year follow-up of an oxidized zirconium femoral prosthesis used for total knee arthroplasty[J]. The Knee,2014,21(1):168-171.
(注,原文标题:电子束粉末床熔融钛合金和多孔钽骨科植入材料的研究及应用进展_郭瑜)
相关链接
- 2026-04-24 激光增材与传统原位制备工艺下非连续增强钛基复合材料的组织性能及应用对比研究——针对激光增材技术在钛基复合材料制备中的创新应用,对
- 2026-04-22 长期高温时效对标准热处理GH4169镍基高温合金δ相析出及综合力学性能的影响研究——以航空领域常用GH4169镍基高温合金为研究载体,采用真
- 2026-04-22 航空用TB17新型超高强韧钛合金固溶–冷却–时效全流程组织调控及其强韧化与劣化机制解析——契合航空装备轻量化高承载长寿命设计发展趋
- 2026-04-19 适配SiC/Ti65复合材料制备的Ti65合金包套组织性能调控及高温服役稳定性优化研究——基于高超声速飞行器前缘、迎风面极端热环境服役需求,
- 2026-04-18 深海装备用Ti75耐蚀钛合金锻件后续热处理微观调控机制及冷热加工全流程性能稳定性优化研究——立足海洋工程钛合金冷热成形焊接后续热加
- 2026-04-14 国内首用Ti55531超高强钛合金起落架横梁制造关键技术攻关与高效精密加工成套技术沉淀——聚焦超高强钛合金工程应用研究空白,突破Ti55531
- 2026-04-13 面向航空承力构件应用的Ti55531近β钛合金相变行为及热激活能研究——通过连续升温热膨胀试验与多手段表征,明确相变序列及升温速率对相变
- 2026-04-10 面向飞机液压管路系统的TA18钛合金管材热处理工艺优化——以冷轧钛管为对象,研究退火对组织回复、再结晶及径向织构的影响,为航空钛合金管
- 2026-04-10 近α型TA15钛合金壳体热挤压成形质量提升机制研究——结合试验与有限元模拟,解析相变温度下坯料表面与中心温差异常导致的黏结裂纹缺陷,通
- 2026-04-04 基于IMI834合金衍生的Ti150高温钛合金大规格棒材固溶温度效应研究——系统分析990~1030℃固溶处理对其等轴/双态组织转变、室温及600℃高

